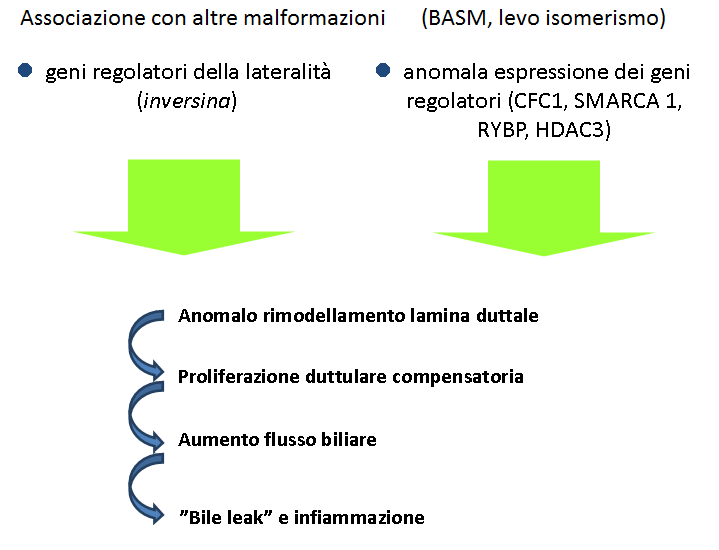
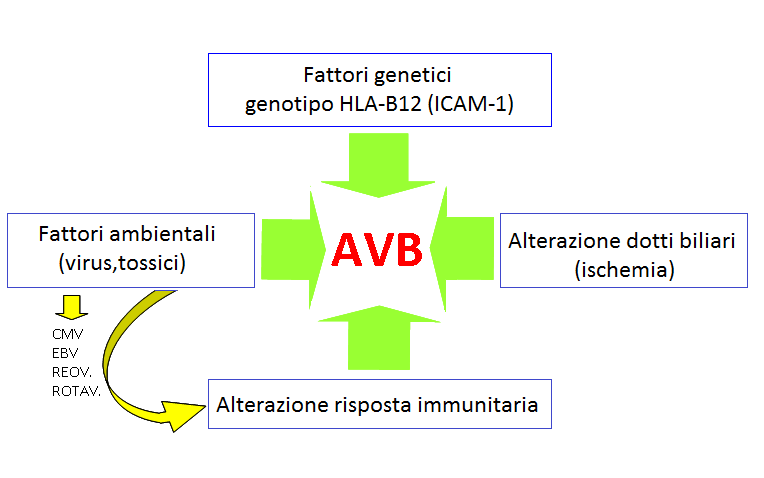
Una delle ipotesi più accreditate sull’eziopatogenesi della AVB è quella di un danno iniziale in epoca pre o perinatale seguito da una risposta infiammatoria non controllata rivolta verso l’epitelio biliare, risultante in un danno progressivo e in una obliterazione dei dotti biliari con cirrosi secondaria.
Sono state proposte diverse ipotesi, ma ad oggi il fattore eziologico, cioè la causa scatenante questa cascata di eventi resta sconosciuta, così come poco chiarito è il meccanismo patogenetico.
Certamente le due forme cliniche di AVB, embrionale/fetale (sindromica) da una parte e perinatale (non sindromica) dall’altra, vedono giocare fattori diversi.
Forma embrionale/fetale
Forma perinatale o acquisita
Molteplici sono i campi di ricerca che sono stati battuti alla ricerca di una causa dell’AVB, ma le ipotesi più studiate sono:
- Un’ipotesi malformativa
- Un’ipotesi virale
- Un’ipotesi immunitaria
Ipotesi malformativa
Tan, confrontando l’aspetto microscopico delle vie biliari alla porta hepatis nel feto di 10-12 settimane e nei pazienti con AVB, ha rilevato notevoli similitudini: da qui l’ipotesi che alcuni casi di AVB possano derivare da alterazioni nel processo di rimodellamento dei dotti biliari o dalla mancata o alterata congiunzione delle primitive vie biliari intraepatiche con quelle extraepatiche.
La persistenza di dotti biliari primitivi di tipo fetale determinerebbe stravaso di bile soprattutto a livello della porta hepatis già a partire dall’inizio della secrezione biliare (12a-13a settimana), con conseguente reazione infiammatoria.
Ruolo dei virus
Per la prima volta nel 1974 Landing propose che l’AVB potesse essere determinata da infezioni virali del fegato e della via biliare; più di recente questa ipotesi è stata supportata da una serie di sperimentazioni su modelli murini. Molti virus sono stati proposti nell’eziologia dell’AVB, ma l’attenzione si è concentrata su reovirus, rotavirus e CytoMegaloVirus (CMV). L’interesse sui reovirus deriva dall’osservazione che topi infettati con questo virus, sviluppano un quadro clinico simili ai pazienti con AVB. Tuttavia, studi sull’uomo hanno dato risultati contrastanti.
Nel 1993 Riepenhoff-Talty per primo descrisse due ceppi di rotavirus che replicavano nel fegato e nelle vie biliari del topo determinando colestasi. In seguito Mack dimostrò che i topi di un giorno infettati con il ceppo Rhesus RotaVirus (RRV) sviluppavano ittero in una settimana e ostruzione biliare e infiammazione portale entro due settimane, nonostante l’eliminazione del virus.
Un recente studio cinese ha identificato il DNA del CMV nel 60% dei pazienti con AVB; Fischler ha dimostrato una elevata prevalenza di anticorpi anti-CMV in madri di pazienti con AVB, alti livelli di IgM anti-CMV nei pazienti e un abbondante deposito di immunoglobuline nella membrana canalicolare degli epatociti in pazienti con AVB e infezione da CMV.
Ruolo della risposta immunitaria
Indipendentemente dal fattore scatenante iniziale, numerose evidenze indicano l’attivazione della risposta immunitaria come fattore chiave nel danno alle vie biliari.
All’inizio degli anni ’80 alcuni Autori avevano dimostrato la presenza di depositi di immunoglobuline lungo la membrana basale dell’epitelio dei dotti biliari nei pazienti con AVB, ponendo l’attenzione sul ruolo dei linfociti B e dell’immunità umorale.
Attualmente la maggior parte degli studi si è concentrata sul ruolo che possono avere i linfociti di tipo T CD4+ e CD8+ presenti negli spazi portali, che producono citochine Th1, e le cellule di Kupffer (macrofagi residenti) che producono TNF-α (Tumor necrosis factors).
La citochina Th1, giocherebbe un ruolo essenziale nel reclutamento delle cellule immunitarie, nella deposizione di matrice extracellulare e nella fibrosi. Inoltre, recentemente è stato ipotizzato che un deficit di linfociti T regolatori (Treg), sarebbe responsabile del mancato controllo dell’attivazione infiammatoria, che risulterebbe eccessiva, con conseguente esacerbazione del danno biliare.
Oggi si pensa che l’AVB presenti sicuramente una eziologia multifattoriale, ossia che più fattori giochino un ruolo determinante, che come ultimo risultato porta alla malformazione delle vie biliari.
ANATOMIA PATOLOGICA
Nell’AVB la via biliare extraepatica e la colecisti si presentano in tutto o in parte ostruite e sostituite da tessuto cicatriziale-fibroso più o meno abbondante.
Il fegato si presenta con un colorito bruno-violaceo e consistenza morbida nelle fasi iniziali, fino a un colore verdastro, consistenza dura, lignea, con superficie irregolare con macro o micronoduli nelle forme avanzate, con evidenti vasi sanguigni e linfatici dilatati, espressione di ipertensione portale, una delle complicanze più temibili dell’AVB.
Microscopicamente il fegato presenta inizialmente lesioni aspecifiche; solo dopo le 4-6 settimane compaiono le tre lesioni tipiche:
- proliferazione di duttuli neoformati alla periferia dello spazio portale
- allargamento degli spazi portali per edema e fibrosi periduttulare
- presenza di trombi biliari nei dotti interlobulari.
A queste lesioni si associano infiltrato infiammatorio nello spazio portale e necrosi cellulare.
Con la progressione della malattia compaiono fenomeni degenerativi dei dotti biliari e progressione della fibrosi, fino ad un quadro conclamato di cirrosi biliare secondaria duttopenica.
Nelle AVB di Tipo 3 nel contesto del tessuto fibroso che ha sostituito i dotti epatici destro e sinistro, sono presenti dei duttuli biliari neoformati (neoduttuli) del diametro che varia tra i 50 e i 300 μm, responsabili del drenaggio biliare dopo l’intervento di porto-enterostomia.
CLINICA
Anamnesi
Pur potendosi raramente verificare in bambini prematuri, il neonato affetto da AVB è solitamente nato a termine e di peso corretto per l’età gestazionale, con un ittero spesso in continuità con quello fisiologico. La gravidanza decorre senza problemi.
Il bimbo di solito si alimenta volentieri e cresce normalmente nelle prime settimane di vita.
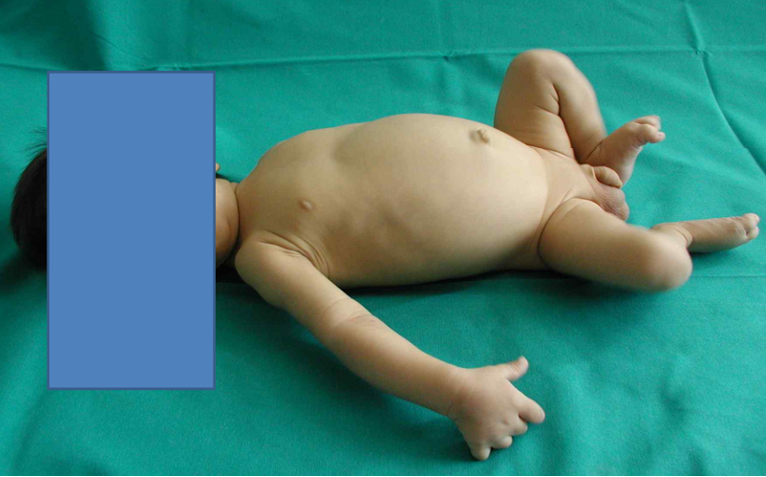
Il primo segno clinico è la comparsa di una ipo-acolia delle feci che diventano poi persistentemente depigmentate: il colore delle feci assume varie gradazioni di bianco-grigiastro, come possiamo vedere, feci molto diverse da quelle giallo oro di un neonato sano;

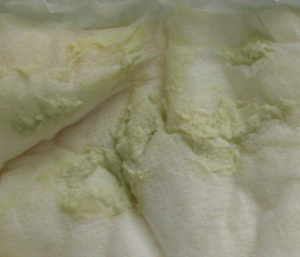
Altro segno è la presenza di urine ipercromiche, che talvolta possono indurre in errore colorando il pannolino e l’esterno delle feci.
Nelle settimane successive può manifestarsi un ritardo di crescita, secondario allo scarso assorbimento di acidi grassi a catena lunga e allo stato catabolico. Lo scarso assorbimento di vitamina K determina inoltre un deficit della coagulazione.
ESAME OBIETTIVO
Solitamente si tratta di un bel bimbo, dall’aspetto sano, se non fosse per la colorazione giallastra delle sclere e della cute: l’Ittero. L’ittero sclero-cutaneo è evidente, con sfumatura verdinica quando la bilirubinemia è molto elevata.
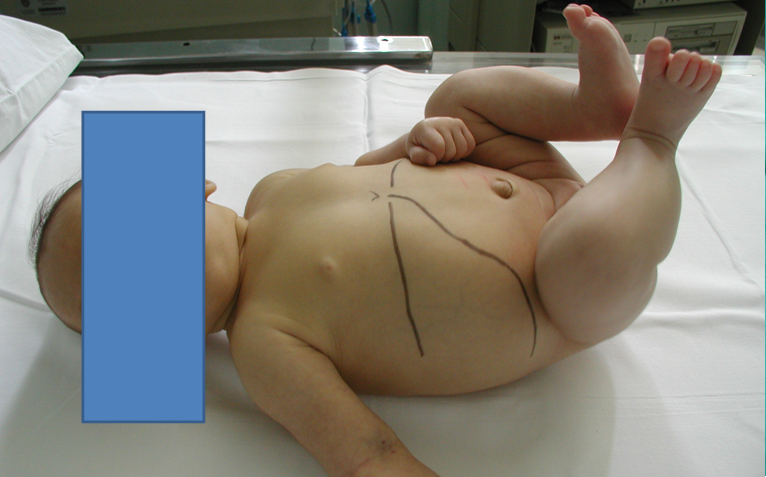
L’epatomegalia (cioè l’ingrossamento del fegato) compare di solito nelle prime settimane di vita, spesso con ipertrofia del lobo di sinistra e consistenza dura, percepibile alla palpazione dell’addome anche da parte dei genitori. Viceversa la splenomegalia (cioè l’ingrossamento della milza) e l’ascite (cioè una anomala raccolta di liquido nella cavità peritoneale) sono reperti tardivi, espressione di una ipertensione portale conclamata.
Agli esami ematochimici di base, prescritti dal Pediatra si evidenzia un incremento della bilirubinemia a prevalente componente diretta, una elevazione delle gamma-GT, della fosfatasi alcalina e delle transaminasi. L’emocromo, gli indici di sintesi epatica come le l’albumina, gli indici di flogosi sono solitamente normali all’esordio.